Dichte und Prozente Kompositionen - Chemie LibreTexts
Einführung
Dichte (\ (\ rho \)) ist eine physikalische Eigenschaft durch Dividieren der Masse eines Objekts durch sein Volumen gefunden. Unabhängig von der Probengröße ist, die Dichte immer konstant. Zum Beispiel ist die Dichte einer Probe von reinen Wolfram immer 19,25 Gramm pro Kubikzentimeter. Das bedeutet, dass, ob Sie ein Gramm oder ein Kilogramm der Probe haben, wird die Dichte nie variieren. Die Gleichung ist wie folgt:
Masse bezieht sich auf die Menge der Materie in einem Objekt. Die SI-Einheit für die Masse ist das Kilogramm (kg), obwohl Gramm (g) wird im Labor häufig verwendet, um kleinere Mengen zu messen. Oft verwechseln Menschen, Gewicht für Masse. Gewicht bezieht sich auf die Kraft, die auf ein Objekt als eine Funktion der Masse und Schwerkraft ausgeübt wird. Dies kann wie folgt geschrieben werden
Daher ändert Gewicht zu Schwankungen der Gravitation und die Beschleunigung aufgrund. Zum Beispiel wird die Masse eines 1 kg Würfel weiterhin 1 kg sein, ob es auf dem Gipfel eines Berges ist, den Grund des Meeres oder auf dem Mond, aber sein Gewicht unterscheiden. Ein weiterer wichtiger Unterschied zwischen Masse und Gewicht ist, wie sie gemessen werden. Das Gewicht wird mit einer Skala gemessen, während Masse mit einer Waage gemessen werden muß. So wie die Menschen Masse und Gewicht zu verwirren, sie verwirren auch Waagen. Eine Balance wirkt die Wirkungen der Schwerkraft, während eine Skala es enthält. Es gibt zwei Arten von im Labor gefunden Salden: elektronische und manuelle. Bei einer manuellen Balance finden Sie die unbekannte Masse eines Objekts durch Einstellen oder Vergleichen bekannten Massen, bis ein Gleichgewicht erreicht ist.
Band beschreibt die Menge von dreidimensionalem Raum als ein Objekt einnimmt. Die SI-Einheit für die Lautstärke ist m in Würfel geschnitten (m 3), aber Milliliter (ml), in Würfel geschnitten Zentimetern (cm 3) und Liter (L) sind häufiger im Labor. Es gibt viele Gleichungen Volumen zu finden. Hier sind nur einige der einfachen diejenigen:
Volumen = (Länge) 3 oder (Länge) (Breite) (Höhe) oder (Grundfläche) (Höhe)
Dichte: Eine weitere Untersuchung
Wir kennen alle die Komponenten der Dichte, also lassen Sie uns an Dichte selbst einen genaueren Blick. Die Einheit am meisten verwendete Dichte auszudrücken, ist g / cm 3 oder g / ml, wenn die SI-Einheit für die Dichte ist technisch kg / m 3 Gramm pro Kubikzentimeter entspricht Gramm pro Milliliter (g / cm 3 = g / ml ). Zur Lösung für die Dichte folgen, einfach der Gleichung d = m / v. Zum Beispiel, wenn Sie Masse 7,0 g und das Volumen von 5,0 cm 3 die Dichte würde einen Metallwürfel mit hatten seine
Manchmal müssen Sie Einheiten konvertieren, um die korrekten Einheiten für die Dichte, wie mg bis g zu erhalten oder in 3 bis 3 cm.
Die Dichte kann verwendet werden, um ein unbekanntes Element zu identifizieren. Natürlich können Sie die Dichte eines Elements in Bezug auf andere Elemente wissen müssen. Unten ist eine Tabelle, die die Dichte der wenige Elemente aus dem Periodensystem bei Standardbedingungen für Temperatur und Druck oder STP auf eine Temperatur von 273 K (0 ° Celsius) und 1 Atmosphäre Druck entsprechenden auflistet.
Element Name und Symbol
Wie aus der Tabelle ersichtlich ist, das dichte Element Osmium (O) mit einer Dichte von 22,6 g / cm 3. Das am wenigsten dichte Element Wasserstoff (H) mit einer Dichte von 0,09 g / cm 3 ist.
Dichte und Temperatur
Tabelle \ (\ Pageindex \): Dichte von Wasser als Funktion der Temperatur
Auch wenn die Regel von Dichte und Temperatur seine Ausnahmen hat, ist es immer noch nützlich. Zum Beispiel erklärt, wie Heißluftballons arbeiten.
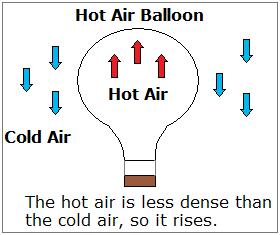
Dichte und Druck

Der griechische Wissenschaftler Archimedes machte eine bedeutende Entdeckung in 212 v.Chr. Die Geschichte geht, dass Archimedes gebeten wurde, für den König um herauszufinden, ob seine Goldschmiedin ihn betrog durch sein Gold für die Krone mit Silber zu ersetzen, ein billigeres Metall. Archimedes wusste nicht, wie das Volumen eines unregelmäßig geformten Objekt zu finden, wie die Krone, obwohl er wusste, dass er zwischen den Elementen durch ihre Dichte unterscheiden. Während in einem Bad auf diesem Rätsel zu meditieren, erkannte Archimedes, als er das Bad betrat, das Wasser stieg. Er erkannte dann, dass er einen ähnlichen Prozess nutzen, um die Dichte der Krone zu bestimmen! Er lief dann angeblich durch die Straßen nackt riefen: „Eureka“, was bedeutet „Ich habe es gefunden!“ in Latein.
Archimedes getestet dann die Krone des Königs durch eine echte Goldkrone gleicher Masse zu nehmen und die Dichten der beiden zu vergleichen. Die Königskrone mehr Wasser als die Goldkrone der gleichen Masse verschoben, dass die Krone des Königs Sinn hatte ein größeres Volumen und somit hatte eine geringere Dichte als die reale Goldkrone. Der Königs „Gold“ Krone wurde daher nicht aus purem Gold. Natürlich ist diese Geschichte heute umstritten, weil Archimedes in all seinen Messungen nicht genau waren, die es schwer, genau zu bestimmen, die Unterschiede zwischen den beiden Kronen machen würde.
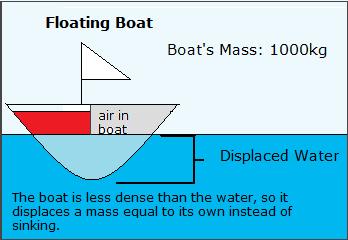
Archimedische Prinzip besagt, dass, wenn ein Objekt eine größere Dichte als die Flüssigkeit, die sie in platziert wird, wird es sinken und verdrängen ein Flüssigkeitsvolumen gleich seinen eigenen. Wenn es eine geringere Dichte hat, wird es schweben und eine Masse von Flüssigkeit gleich seinen eigenen verdrängen. Wenn die Dichte gleich ist, wird es nicht sinken oder schwimmen. Dieses Prinzip erklärt auch, warum Ballons mit Helium gefüllt Schwimmer. Luftballons, wie wir im Abschnitt gelernt über Dichte und Temperatur, Schwimmer, weil sie weniger dicht als die umgebende Luft sind. Helium ist weniger dicht als die atmosphärische Luft, so dass es steigt. Archimedische Prinzip kann auch verwendet werden, um zu erklären, warum Boote schweben. Boote, einschließlich aller Luftraum, im Rahmen ihrer Rümpfe, sind weit weniger dicht als Wasser. Boote aus Stahl kann schweben, weil sie ihre Masse in Wasser verdrängen, ohne den ganzen Weg eingetaucht.
Tabelle \ (\ Pageindex \) unten gibt die Dichten von einigen Flüssigkeiten Dinge in die richtige Perspektive zu setzen.
Prozentuale Zusammensetzung
Schritte zum Berechnen der prozentualen Zusammensetzung der Elemente in einer Verbindung
- Findet die Molmasse aller Elemente in der Verbindung in Gramm pro Mol.
- Finden Sie die molekulare Masse der gesamten Verbindung.
- Dividieren die Molmasse der Komponente durch die gesamte Molekülmasse.
- Sie haben nun eine Zahl zwischen 0 und 1. Multiplizieren mit 100% er prozentuale Zusammensetzung zu erhalten.
Tipps zur Lösung:
- Die prozentuale Zusammensetzung aller Elemente in einer Verbindungen müssen bis zu 100% addieren. In einer binären Verbindung, können Sie das% des ersten Elements finden können, tun Sie dann 100% - (% erstes Element) zu erhalten (% zweites Element)
- Wenn ein Rechner verwenden, können Sie den gesamten Molmasse zu einer Variablen speichern, wie beispielsweise „A“. Das beschleunigt die Berechnungen und Fehler reduzieren.
Beispiel \ (\ Pageindex \): Phosphorpenta
Was ist die prozentuale Zusammensetzung von Phosphor und Chlor in \ (PCl_5 \)?
Findet die Molmasse aller Elemente in der Verbindung in Gramm pro Mol.
Finden Sie die molekulare Masse der gesamten Verbindung.
- \ (PCl_5 \): \ (1 \ times 30,975 \, g / mol + 5 \ times 35,453 \, g / mol = 208,239 \, g / mol \)
Dividieren die Molmasse der Komponente durch die gesamte Molekülmasse.
Daher kann in \ (PCl_5 \) ist 14,87% Phosphor und 85,13% Chlor Massen.
Beispiel \ (\ Pageindex \): HCl
Was ist die prozentuale Zusammensetzung jedes Elements in Salzsäure (HCl).
Zuerst finden die Molmasse von Wasserstoff.
Nun findet die molekulare Masse des HCl-Moleküls:
\ [1,00794 \, 35,4527 g + \, g = 36,46064 \, g \]
Führen Sie die Schritte 3 und 4:
Nun subtrahiert nur in der Verbindung mit den Masseprozent Chlor zu finden:
Daher \ (HCl \) ist 2,76% Wasserstoff und 97,24% Chlor Massen.
Prozent Zusammensetzung im Alltag
Nutrition Labels

Penny: The Lucky Kupfermünze
Der Groschen sollte „das glückliche Kupfer beschichtet Münze“ bezeichnet werden. Der Groschen ist aus massivem Kupfer nicht, da ein Teil von 1857. Nach 1857 gemacht wurden, begann die US-Regierung das Hinzufügen andere billigere Metalle in den Mix. Der Groschen, nur ein Cent zu sein, ist buchstäblich nicht wert sein Gewicht in Kupfer. Die Menschen könnten Kupfer Pennies und verkaufen das Kupfer für mehr als die paar Cent wert waren schmelzen. Nach 1857 wurde Nickel mit dem teureren Kupfer gemischt. Nach 1864 wurde der Groschen aus Bronze. Bronze ist 95% Kupfer und 5% Zink und Zinn. Seit einem Jahr 1943 hatte der Groschen kein Kupfer darin aufgrund der Kosten des Zweiten Weltkrieges. Es wurde nur Stahl beschichtet Zink. Nach 1943 bis 1982 ging der Groschen durch Zeiten, in denen es Messing oder Bronze war.

Heute ist der Groschen in Amerika 2,5% Kupfer mit 97,5% Zink. Die Kupfermäntel der Außenseite des Cent, während der innere Abschnitt Zink ist. Zum Vergleich willen, ist der Groschen in Kanada 94% Stahl, 1,5% Nickel und 4,5% Kupfer.
Unten ist ein Bild von einem zerkratzten Cent vor und nach dem es in Zitronensaft getaucht worden war. Zitronensaft hat einen ähnlichen pH-Wert von 1,5 bis 2,5, wenn sie den normalen menschlichen Magen Vergleich nach Nahrung verbraucht wurde. Verstrichene Zeit: 36 Stunden.


Wie Sie sehen können, ist das Kupfer stark unversehrt durch den Zitronensaft. Deshalb vor 1982 gemacht Pennies mit hauptsächlich Kupfer (mit Ausnahme des 1943 Penny) sind relativ sicher zu schlucken. Die Chancen stehen gut sie durch das Verdauungssystem natürlich passieren würde, bevor ein Schaden getan werden könnte. Doch es ist klar, dass das Zink teilweise aufgelöst wurde, obwohl es nur für eine begrenzte Zeit in der Zitronensaft war. Daher ist die prozentuale Zusammensetzung der Post 1982 Pennies gefährlich für Ihre Gesundheit und die Gesundheit Ihrer Haustiere, wenn sie verschluckt.
Dichte und die prozentuale Zusammensetzung sind wichtige Konzepte in der Chemie. Jeweils Basiskomponenten sowie eine breite Anwendung. Die Komponenten der Dichte: Masse und Volumen, die beide mehr verwirrend als auf den ersten Blick sein kann. Eine Anwendung des Konzepts der Dichte ist die Bestimmung des Volumens einer unregelmäßigen Form, die eine bekannte Masse und Dichte verwendet. Prozentuale Zusammensetzung der Bestimmung erfordert die Masse der gesamten Objekts oder Moleküls und die Masse der Komponenten zu kennen. Im Labor kann, Dichte verwendet werden, um ein Element zu identifizieren, während der prozentuale Zusammensetzung verwendet wird, die Menge, Masse, um zu bestimmen, jedes Element in einer chemischen Verbindung. Im täglichen Leben, erklärt Dichte alles von warum Booten schweben, warum werden versuchen, Luftblasen aus Soda zu entkommen. Es wirkt sich auch Ihre Gesundheit, weil die Knochendichte ist sehr wichtig. In ähnlicher Weise wird prozentuale Zusammensetzung üblicherweise in Ihrer Küche gefunden machen Tierfutter und Verbindungen wie Backpulver verwendet.
Dichte Probleme
Diese Probleme sollen am Anfang einfach sein und dann allmählich schwieriger. Sofern nicht anders angegeben, sollten Antworten in g / ml oder das Äquivalent g / cm 3 sein.
- Wenn Sie eine 2.130-ml-Probe von Essigsäure mit Masse 0,002234 kg haben, was die Dichte?
- Berechnen der Dichte eines 0,03020 L Probe von Ethylalkohol mit einer Masse von 23,71002 g.
- Finden Sie die Dichte einer Probe, die ein Volumen von 36,5 L und eine Masse von 10,0 kg hat.
- Um ein Volumen in ml eines Objekts, das eine Dichte von 10,2 g / l und eine Masse von 30,0 kg aufweist.
- Berechnen Sie die Masse in Gramm eines Objekts mit einem Volumen von 23,5 ml und eine Dichte von 10,0 g / L.
- Berechnen der Dichte eines rechteckigen Prismas aus Metall. Die Abmessungen des Prismas sind: 5cm von 4cm von 5cm. Das Metall hat eine Masse von 50 Gramm.
- Finden Sie die denstiy einer unbekannten Flüssigkeit in einem Becher. Die Masse des Bechers ist 165g, wenn keine Flüssigkeit vorhanden ist. Mit der unbekannten Flüssigkeit, die Gesamtmasse 309g. Das Volumen des Unbekannten ist 125 ml.
- Bestimmen Sie die Dichte in g / l einem unbekannten mit den folgenden Informationen. Ein 55 Gallonen Wanne wiegt 137.5lb, wenn sie leer und 500,0 lb, wenn sie mit dem Unbekannten gefüllt.
- Ein Ring hat eine Masse von 5,00 g und ein Volumen von 0.476 ml. Ist es reines Silber?
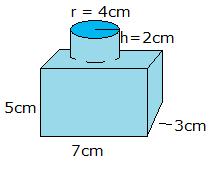
- Was ist die Dichte des Feststoffs in dem Bild, wenn die Masse 40 g ist? Machen Sie Ihre Antwort 3 signifikante Zahlen haben.
11) Im Folgenden ist ein Modell einer Pyramide an einer archäologischen Ausgrabungs gefunden aus einer unbekannten Substanz. Es ist zu groß, um die Lautstärke zu finden, indem es in Wasser eingetaucht. Auch weigern sich die Wissenschaftler ein Stück zu entfernen, zu testen, da diese Pyramide ein Teil der Geschichte ist. Seine Höhe beträgt 150,0 Mio.. Die Länge seiner Basis ist 75,0 und die Breite ist 50.0m. Die Masse dieser Pyramide ist 5.50x10 5 kg. Was ist die Dichte?
Dichte Problemlösungen
Prozentuale Zusammensetzung Probleme
Diese Probleme werden das gleiche Muster von Schwierigkeiten wie die der Dichte folgen.
- Berechnen Sie den Massenprozent jedes Elements in Caesiumfluorid (CsF).
- Berechnen Sie die Massenprozent jeden Element in Kohlenstofftetrachlorid (CCl4)
- Eine Lösung aus Salz und Wasser 33,0% Salz durch Masse und hat eine Dichte von 1,50 g / ml. Welche Masse des Salzes in Gramm ist in 5,00 l dieser Lösung?
- Eine Lösung aus Wasser und HCl enthält 25% HCl Massen. Die Dichte der Lösung beträgt 1,05 g / ml. Wenn Sie 1,7 g HCl für eine Reaktion benötigen, welche Volumen dieser Lösung werden Sie verwenden?
- Eine Lösung, 42% NaOH Masse- enthält, eine Dichte von 1,30 g / mL. Welche Masse in Kilogramm NaOH in 6,00 l dieser Lösung?
Prozent Zusammensetzung Problemlösungen
- CsF ist 87,5% und 12,5% Cs F Masse-
- CCl4 beträgt 92,2% Cl und 7,8% C Massen
- 2480g
- 6,5 ml
- 2,38 kg
Referenzen
Tate, J. "Archimedes’ Entdeckungen: Ein genauerer Blick."
- Es gibt keine empfohlenen Artikel.
